Article /
LE POINT SUR L’ENDODONTIE DE DEMAIN
Maxime Ducret, Audrey Aussel
L’endodontie et les traitements conventionnels : Plusieurs limites actuelles
La gestion des infections endodontiques est courante dans notre exercice de chirurgien-dentiste.
D’étiologies diverses, elles impliquent majoritairement la réalisation d’un traitement endodontique
conventionnel. Cependant, dans le cadre de la dent permanente immature (DPI), ce traitement ne peut
pas être utilisé. En effet, la DPI présente encore un apex ouvert, ne permettant pas d’assurer une
barrière pour le matériau d’obturation radiculaire. La majorité des praticiens ont donc recours à une
procédure d’apexification. Elle permet la création d’une barrière apicale, notamment par le placement
immédiat d’un bouchon apical de MTA® ou de Biodentine®. Cependant, cette technique induit un arrêt
de l’édification radiculaire et participe au risque de survenue de fractures (1).
L’endodontie et les thérapies régénératrices : Un concept alternatif
Une meilleure compréhension des mécanismes biologiques à l’interface tissu /biomatériau a permis
progressivement de développer des stratégies plus efficientes et ainsi pallier les limites des traitements
conventionnels. De nouvelles thérapies dites « régénératrices » ont été proposées, avec pour objectif
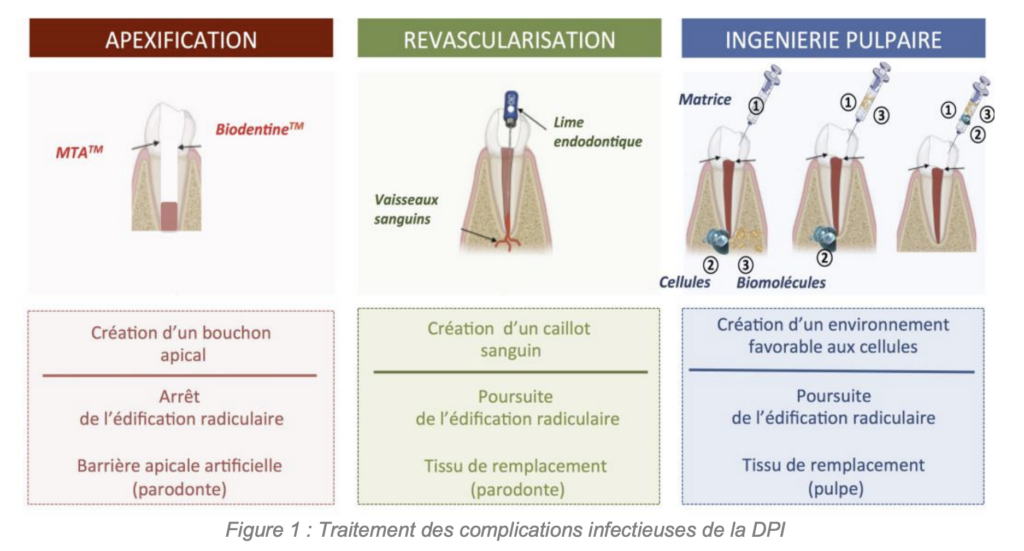
d’induire le remplacement du tissu lésé par un néo tissu fonctionnel (2). Deux concepts sont ainsi
proposés : la « revascularisation » et l’ingénierie pulpaire, en opposition à l’apexification (Figure 1).
La revascularisation est un procédé qui consiste à induire la formation d’un caillot sanguin au sein
du canal désinfecté, à l’aide d’une lime endodontique. Théoriquement, ce caillot favorise le recrutement
cellulaire et apporte une source de facteurs de croissance et de cellules souches. Ces facteurs de
croissance pourraient stimuler la croissance et la différenciation de cellules souches notamment du
ligament parodontal et de la papille apicale. La revascularisation permet la poursuite de l’édification
radiculaire et pallier les limites mécaniques de l’apexification. Cependant, le tissu formé au sein d’un
canal reste plus proche d’un tissu parodontal que d’un tissu pulpaire (3). L’ingénierie pulpaire a donc
été développée afin de pallier ces limites, en assurant la poursuite de l’édification radiculaire et en
permettant l’élaboration d’un tissu proche de la pulpe. Basé sur les principes de l’ingénierie tissulaire,
il s’agit d’utiliser matrices, cellules, biomolécules, associées ou non selon les différentes stratégies (4,
5). La recherche dans ce domaine est en plein essor et fait l’objet de nombreuses publications, cliniques
et pré-cliniques, notamment sur la mise au point de nouvelles matrices. En effet, cette matrice a un rôle
central, car elle sert d’échafaudage aux cellules, tout permettant de garantir l’activité et la
communication entre ces dernières. Elle assure également un maintien pendant une durée suffisante
pour régénérer le tissu.
La Recherche en France en ingénierie pulpaire : L’exemple du projet CAM-RET
En 2022, le projet CAM-RET a été initié grâce au soutien de l’Institut Français pour la Recherche en
Odontologie (IFRO). Ce projet est le fruit d’une récente collaboration entre deux partenaires
académiques spécialisés dans le domaine de l’ingénierie thérapeutique, BioTis (INSERM, Bordeaux) et
LBTI (CNRS, Lyon). La finalité était de réunir ces deux laboratoires, et de bénéficier de leur l’expertise
dans le domaine de l’ingénierie tissulaire pulpaire et vasculaire. L’objectif principal de ce projet était
d’utiliser de la matrice extra-cellulaire obtenue à partir de fibroblastes humains (CAM) comme une
matrice innovante et originale pour l’ingénierie pulpaire. Au cours des 15 dernières années, cette
matrice a été caractérisée et produite sous différentes formes (6, 7), principalement pour des
applications cliniques sur l’ingénierie de vaisseaux sanguins (8-11). De par ses excellentes propriétés
biologiques et mécaniques, ce projet cherchait à évaluer la faisabilité de faire de l’ingénierie pulpaire à
partir de la CAM. En ingénierie pulpaire, la matrice idéale doit répondre à un cahier des charges précis,
notamment en termes de propriétés biologiques, mécaniques et physiques. Cette matrice doit
notamment permettre une manipulation aisée pour une mise en place rapide dans l’espace
endodontique (en quelques minutes), avoir une faible viscosité pour une bonne injectabilité dans un
espace aussi réduit que le canal dentaire, des propriétés antibactériennes pour empêcher la croissance
de bactéries endodontiques résiduelles, une dégradation par l’hôte, et un remplacement rapide par une
matrice extra-cellulaire (MEC) caractéristique du tissu pulpaire dentaire (4). Pour répondre à ces
exigences, divers biomatériaux ont été développés et sont rapportés dans la littérature, comme les
polymères synthétiques, naturels, les biocéramiques et dérivés et la MEC et ses composants. La CAM,
catégorisée dans les dérivés de la MEC, pourrait être considérée comme une matrice prometteuse. En
effet, elle fournit un environnement dynamique, notamment des signaux biochimiques et mécaniques
permettant de guider le comportement cellulaire et elle peut être sélectivement dégradée et remodelée.
Cependant, il peut être difficile d’obtenir une faible viscosité, compromettant l’injectabilité dans l’espace
endodontique (5). L’association de fibrine à la CAM pourrait permettre d’obtenir un produit issu de
l’ingénierie pulpaire innovant et adapté (12-14). D’après les premiers résultats du projet, la CAM
semblerait prometteuse pour l’ingénierie pulpaire, en offrant un environnement favorable à la croissance
et à la migration de cellules souches vasculaires et de la papille apicale.
La Recherche en France en ingénierie pulpaire : Un réseau de laboratoires et odontologistes
En 2019, en collaboration avec la conférence des doyens, l’Institut Français pour le Recherche en
Odontologie (IFRO) a réalisé une cartographie actualisée des laboratoires de recherche en France
métropolitaine intégrant un chercheur odontologiste ou ayant une thématique de recherche en lien avec
l’odontologie (15). 88 laboratoires ont été répertoriés, dont les thématiques de recherche sont variées
et majoritairement en lien avec les technologies pour la santé (37 %), notamment le domaine des
biomatériaux. Au sein de ces laboratoires, plusieurs équipes travaillent sur la thématique de l’ingénierie
tissulaire. Ce réseau national de recherche en odontologie est une véritable force pour notre profession
dans sa recherche d’excellence et d’innovation, mais également pour accompagner cette évolution du
métier, qui nous amènera sans aucun doute vers une odontologie qui régénère et reconstruit les tissus
avec et pour la biologie.
En conclusion, l’endodontie de demain est déjà celle d’aujourd’hui avec des techniques
applicables en cabinet dentaire, comme la revascularisation. Cependant, les nombreuses
recherches initiées dans le domaine et notamment en France, laissent encore espérer des
évolutions. Une meilleure compréhension de la biologie et la mise au point de biomatériaux
alliant propriétés mécaniques et biologiques adéquates laissent permettront la création d’un
environnement favorable à la régénération pulpaire et in fine la régénération d’une pulpe dentaire
ad integrum.
ABRÉVIATIONS
- CAM matrice extra-cellulaire obtenue à partir de fibroblastes humains
- DPI dent permanente immature
- IFRO Institut Français pour la Recherche en Odontologie
- MEC matrice extracellulaire
- MTA Mineral Trioxide Aggregate®
RÉFÉRENCES
Duggal M, et al. 2017 Interventions for the endodontic management of non-vital traumatised
immature permanent anterior teeth in children and adolescents: a systematic review of the evidence
and guidelines of the European Academy of Paediatric Dentistry European Archives of Paediatric
Dentistry. 18 139-51
Liu H, et al. 2022 Biomaterial scaffolds for clinical procedures in endodontic regeneration Bioact
Mater. 12 257-77
Siddiqui Z, et al. 2022 Cells and material-based strategies for regenerative endodontics Bioact
Mater. 14 234-49
Dissanayaka WL, et al. 2020 Scaffold-based and Scaffold-free Strategies in Dental Pulp
Regeneration Journal of Endodontics. 46 S81-S89
Moussa DG, et al. 2019 Present and future of tissue engineering scaffolds for dentin-pulp
complex regeneration 13 58-75
Magnan L, et al. 2020 Human textiles: A cell-synthesized yarn as a truly « bio » material for tissue
engineering applications Acta Biomater. 105 111-20
Magnan L, et al. 2018 Characterization of a Cell-Assembled extracellular Matrix and the effect
of the devitalization process Acta Biomaterialia. 82 56-67
L’Heureux N, et al. 2006 Human tissue-engineered blood vessels for adult arterial
revascularization Nat Med. 12 361-5
McAllister TN, et al. 2009 Effectiveness of haemodialysis access with an autologous tissue
engineered vascular graft: a multicentre cohort study Lancet. 373 1440-6
Wystrychowski W, et al. 2014 First human use of an allogeneic tissue-engineered vascular graft
for hemodialysis access J Vasc Surg. 60 1353-57
Wystrychowski W, et al. 2011 Case study: first implantation of a frozen, devitalized tissue
engineered vascular graft for urgent hemodialysis access J Vasc Access. 12 67-70
Ducret M, et al. 2021 Fibrin-based scaffolds for dental pulp regeneration: from biology to
nanotherapeutics Eur Cell Mater. 41 1-14
Ducret M, et al. 2017 Current challenges in human tooth revitalization Biomed Mater Eng. 28
S159-s68
Ducret M, et al. 2019 Design and characterization of a chitosan-enriched fibrin hydrogel for
human dental pulp regeneration Dent Mater. 35 523-33
Pers J-O, et al. 2019 Les Unités de recherche en lien avec la filière odontologique. Cartographie
française Information Dentaire 12 28-38
Collaboration
LBTI (INSERM, Lyon)
Ducret Maxime (PU-PH)
Jean-Christophe Farges (PU-PH)
Mourad Bekhouche (MCU)
Marianne Leveque (PhD)
Camille Girolet (M2)
BioTis (CNRS, Bordeaux)
Audrey Aussel (MCU-PH)
Nicolas L’Heureux (DR1)
Olivia Kerouredan (MCU-PH)
Atena Ourdas (M2)
